在介绍了细胞凋亡、细胞自噬、细胞坏死、坏死性凋亡、细胞焦亡、铁死亡以及铜死亡这些细胞花式死法之后,我们的细胞死亡大盘点系列迎来了最终章——双硫死亡。
双硫死亡的定义
双硫死亡,是一种由过量胱氨酸积累引起的二硫化物应激(Disulfide stress)导致的新型细胞死亡类型,在2023年3月 《Nature Cell Biology》 杂志上的研究论文Actin cytoskeleton vulnerability to disulfide stress mediates disulfidptosis中被首次报道。

图1. 《Nature Cell Biology》文献截图
研究发现,葡萄糖匮乏诱导的SLC7A11高表达癌细胞的细胞死亡不属于任何一种已知的细胞死亡类型。这种新的细胞死亡类型不能被一般用于抑制细胞死亡的药物抑制,也不能通过敲除铁死亡/细胞凋亡关键基因来阻止。而硫醇氧化剂(如二酰胺和马来酸二乙酯)则可以显著增强这种细胞死亡,因此这种细胞死亡形式被命名为双硫死亡。
进一步研究发现,双硫死亡的主要原因是NADPH的供应不能满足细胞将胱氨酸还原成为半胱氨酸的过程,造成二硫化物应激,诱导肌动蛋白细胞骨架蛋白二硫键形成、细胞骨架收缩以及与细胞质膜的剥离,并最终导致细胞死亡。细胞葡萄糖摄入不足和胱氨酸摄入过量都可能诱导双硫死亡。
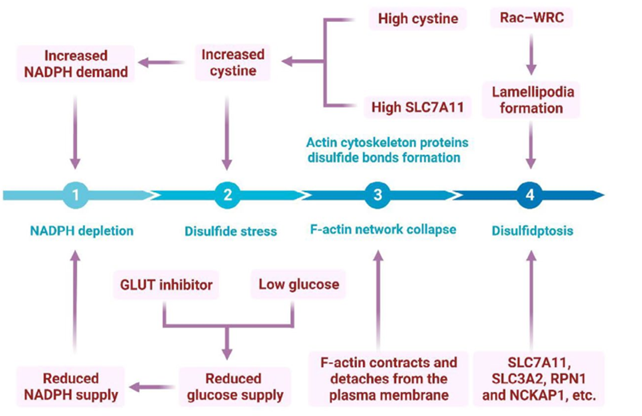
图2. 双硫死亡发生的过程
双硫死亡的机制
双硫死亡是一种通过氧化还原反应和二硫键形成触发细胞死亡的程序性细胞死亡方式。根据已有文献,双硫死亡涉及到的调控途径有胱氨酸摄取和葡萄糖代谢途径,可由胱氨酸转运蛋白溶质载体家族7成员11(SLC7A11,也称为xCT)、NCKAP1等蛋白质和二硫还原剂、2-DG等化合物调节,其中主要的关键因子是SLC7A11。
SLC7A11的作用是将胞外胱氨酸装运到细胞内。胱氨酸是合成谷胱甘肽、抑制细胞氧化应激的重要原料之一,但其本身也具有一定的细胞毒性。胱氨酸是一种不溶性氨基酸,为了防止细胞内高度不溶性胱氨酸的毒性积聚,细胞需要迅速将胱氨酸还原为半胱氨酸,而这个过程需要从葡萄糖-戊糖磷酸途径(PPP)获得大量NADPH,这会对细胞NADPH库造成大量消耗,并使此类细胞产生葡萄糖和戊糖磷酸途径(PPP)依赖性。当细胞存在SLC7A11高表达时,会引起胱氨酸摄取增加,进而引起NADPH供应不足,最终可能导致细胞死亡。

图3. 双硫死亡的机制
双硫死亡的研究进展
目前关于双硫死亡的研究处于生信分析阶段,其被认为是可用于癌症治疗的一种新的调节性细胞死亡形式。由于SLC7A11在许多癌症中都是高表达的,所以在不影响正常细胞的情况下,可能存在抑制葡萄糖转运蛋白,并存在这些细胞中诱导双硫死亡的窗口。另外,有研究显示,与双硫死亡的相关的新生物标志物可用于肝癌的临床诊断,预测预后及治疗靶点。而在心肌梗死和卒中等疾病中,抑制双硫死亡已被证明可减轻损伤。因此,双硫死亡的发现有望治疗那些逃避其它疗法并对细胞凋亡有抵抗力的癌症,需要进一步的研究和探索。
双硫死亡的检测方式
双硫死亡的特征有胱氨酸增加、双硫分子增加、细胞收缩和 F-肌动蛋白收缩等,根据这些特征,铁死亡的判断与检测,可以通过四个方面进行检测:代谢检测、形态检测、蛋白检测和基因检测。
⋆ 代谢检测:NADPH、ATP、胱氨酸摄取、葡萄糖、Trx等。
⋆ 形态检测:染色检测肌动蛋白丝的形态。
⋆ 蛋白检测:GLUT1、GLUT3、HK2、LDHA、SLC7A11。
⋆ 基因检测:GSTT1、MYH9、NCKAP1、RPN1。
Elabscience®双硫死亡检测试剂
|
相关指标 |
货号 |
产品名称 |
|
细胞活力 | E-CK-A362 |
|
|
E-BC-K771-M |
||
|
胱氨酸摄取 | E-BC-F066 |
|
|
ATP |
E-BC-K157-M |
|
|
E-BC-F002 |
||
|
ROS |
E-BC-K138-F |
|
|
LPO |
E-BC-F003 |
|
|
E-BC-K176-M |
||
|
NADP+/NADPH |
E-BC-K803-M |
|
|
葡萄糖 |
E-BC-K234-M |
|
|
E-BC-F037 |
||
|
葡萄糖摄取 |
E-BC-F041 |
|
|
G6P |
E-BC-K011-M |
|
|
G6PDH |
E-BC-K056-M |
点击货号查看产品详情
本期关于双硫死亡的知识就介绍到这里了,至此,细胞死亡大盘点系列将暂时告一段落~
相关阅读:一种新的细胞死亡方式——双硫死亡