在之前的“ 细胞死亡大盘点 ”系列(戳蓝字回顾往期知识点)推文中,我们了解了细胞凋亡、细胞自噬、细胞坏死、坏死性凋亡、细胞焦亡、铁死亡、铜死亡、双硫死亡的相关内容。今天带大家继续探寻又一复杂的细胞死亡方式——泛凋亡。
什么是泛凋亡?
泛凋亡(PANoptosis)是2019年由美国学者Malireddi等[1]提出的一种全新程序性死亡方式。泛凋亡受到PANoptosome(泛凋亡体)复合物的调控,具有细胞焦亡(Pyroptosis)、凋亡(Apoptosis)和/或坏死性凋亡(Necroptosis)的关键特征,这也是PANoptosis术语中“P”、“A”和“N”的来源,但泛凋亡却不能用这3种程序性细胞死亡(PCD)途径单独解释。
以往的研究中,一般认为凋亡、焦亡、坏死性凋亡三者都是独立运行的,但是随着研究的深入,越来越多的研究结果表明这三者之间存在着某种串扰,它们之间可以相互交叉调节。如:凋亡执行者Caspase-3和Caspase-7可以通过氨基端分裂灭活GSDMD,还可以裂解GSDME,使细胞死亡的形态由凋亡转变为焦亡;坏死性凋亡的执行和MLKL孔的形成可通过膜损伤激活细胞凋亡。这些发现促成了PANoptosis(泛凋亡)概念的建立。
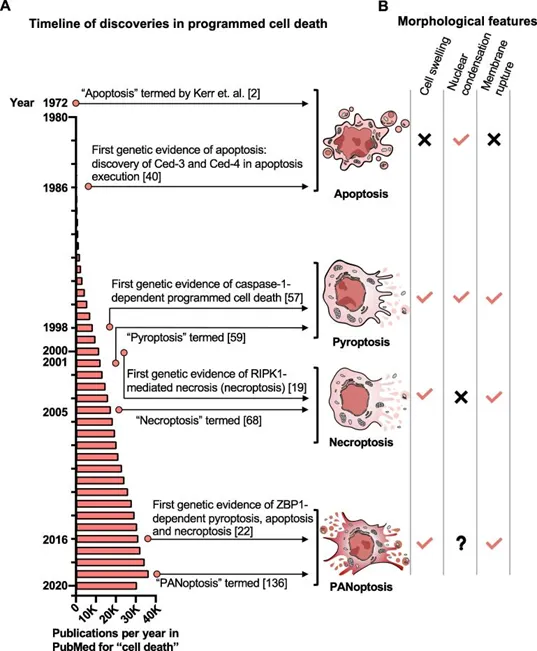
图1. 细胞凋亡、细胞焦亡、坏死性凋亡和 PANoptosis 的关键里程碑
参考文献:10.1016/j.csbj.2021.07.038
泛凋亡调控
泛凋亡受到上游感受器和分子信号的级联调控,这些传感器和级联信号组装成一种多聚体复合物,即泛凋亡小体(PANoptosome)[2]。作为下游分子的激活平台和启动3种PCD途径的“总开关”,PANoptosome及其上游的感受器为人类疾病的治疗提供了颇具吸引力的干预靶点[3]。已经明确的泛凋亡上游分子有三种,分别是 ZBP1、RIPK1 和 AIM2,它们可以感受特定刺激并触发泛凋亡小体的组装,形成三种具有不同传感器和调节因子的泛凋亡小体,即 ZBP1-PANoptosomes、AIM2-PANoptosomes 和 RIPK1-PANoptosomes。

图2. 泛凋亡小体及其通路
参考文献:10.3760/cma.j.cn112137-20220128-00213.
泛凋亡小体的形成
尽管不同病原体感染激发的近端感受器存在差异,但这些感受器分子均可启动泛凋亡小体的形成。后者提供了一个分子支架,允许焦亡[NLRP-3、凋亡相关的含有CARD结构域的斑点状蛋白(apoptosis-associated speck-like protein containing a CARD,ASC)和Caspase-1]、凋亡(Caspase-8/3)和坏死性凋亡(RIPK3,p-MLKL)所需的蛋白或分子进行耦联和结合[4]。迄今为止,已经明确的泛凋亡上游分子有三种,分别是ZBP1、RIPK1和干扰素诱发蛋白2(interferon-inducible protein 2,AIM2),它们可以感受特定刺激并触发泛凋亡小体的组装,但上游感受器如何特异性识别病原微生物感染以及这些成分之间相互作用的具体机制依旧未知。此外,研究表明应该还有其他上游分子可启动泛凋亡。
泛凋亡检测方法及指标
观察细胞形态:细胞焦亡引起细胞质肿胀和膜破裂;凋亡主要形态学特征包括染色质固缩、DNA 片段化、细胞膜起泡、细胞皱缩、凋亡小体的形成等。
检测不同 PCD 的关键蛋白:焦亡相关: Caspase-1 、 Caspase-4 、 GSDMD 、 AIM2 /Pyrin/NLRP3 等,凋亡相关: Caspase-3 、 Caspase-7 、 Caspase-8 、 PARP 、 Bax /Bcl 等,坏死性凋亡相关: MLKL 、 RIPK1 、RIPK3、 ZBP1 等。
其他检测方法: Annexin V 、 TUNEL 、 JC-1 等方法检测凋亡;ELISA 检测炎症因子的释放;免疫印迹、流式等技术检测炎性小体NLRP3 表达和Caspase活化情况。
泛凋亡可以说是目前已知最复杂的细胞死亡形式,既包含细胞焦亡、细胞凋亡和坏死性凋亡的特征,又不能被任何单一死亡形式表征,具有极高的研究价值和前景。